![]() 《化学与生活》测试
《化学与生活》测试
1、单选题(每小题只有一个正确答案)
1.食用低钠高钾盐,可以预防高血压。减少心脑血管疾病的发生率。这里的“钠”“钾”指的是()
A.原子 B.离子 C.元素 D.单质
2.下列食物中主要为人体提供蛋白质的是
A.牛油 B.蔬菜 C.米饭 D.牛奶
3.低血糖病人天天应注意摄入适量的淀粉等化合物,以保持血液中的葡萄糖浓度肯定。食用下列食品,可以较好地预防低血糖的是
①大米饭②花生仁③土豆片④玉米粥⑤鲜牛奶
A.①②⑤ B.①③④ C.②③④ D.①③④⑤
4.张红同学出现了腹泻的症状,大夫建议暂时不吃富含蛋白质和油脂的食物,张红同学应该选择的早餐是()
A.油条和豆浆 B.鸡蛋和牛奶 C.馒头和稀饭 D.肯德基和酸奶
5.“饭遭殃”是綦江的一种品牌食品,制作材料包括了以下物质,其中富含油脂的是
A.花生 B.味精 C.辣椒 D.瘦牛肉
6.学校饭店提供了下列5种食物,茜茜为自己安排的午餐菜谱中,较适当的是

A.①②③ B.①③④ C.②④⑤ D.③④⑤
7.下列说法正确的是( )
A.煤是可再生能源
B.人体缺碘会引起甲状腺肿大
C.蛋白质是人体的主要供能物质
D.乙醇汽油作汽车燃料不会污染环境
8.食品安全问题日益成为社会关注的焦点。下列有关认识正确的是
A.用亚硝酸钠增加食物的鲜味 B.用小苏打作油条膨松剂
C.用火碱“洗白”海参、鱿鱼 D.用霉变的大豆制作豆腐
9.分类法是化学学习和研究的要紧办法之一,下列分类正确的是( )
A.复合肥料:尿素、硝酸钾、磷酸氢二铵 B.氧化物:水、氯酸钾、五氧化二磷
C.碱:纯碱,石灰水,苛性钠 D.合成材料:塑料,合成橡胶,合成纤维
10.民生热词:“舌尖上的安全”。下列做法符合食品安全需要的是()
A.用碳酸氢钠作发酵粉 B.用甲醛浸泡水商品
C.用亚硝酸钠代替食盐烹调食物 D.为预防骨质疏松,长期摄入过量的钙元素
11.下列食品中,富含糖类的是 ( )
A.鸡蛋 B.黄瓜 C.豆油 D.玉米
12.下列物质中,不是有机物的是
A.碳酸钙 B.甲烷 C.乙醇 D.葡萄糖
13.下列用品中的塑料是热固性塑料的是
A.电器插座 B.塑料垃圾篓 C.塑料袋 D.塑料桶
14.下列实验现象与讲解不相符的是
| 实验 | 现象 | 讲解缘由 |
A | 吹灭蜡烛 | 产生一缕白烟 | 石蜡蒸汽遇冷凝固 |
B | 酒精与水混合 | 总体积变小 | 分子之间有空隙 |
C | 硝酸铵溶于水 | 溶液温度减少 | 硝酸铵溶于水吸热 |
D | 鸡蛋清中加乙酸铅溶液 | 产生白色沉淀 | 蛋白质溶解性变小 |
A.A B.B C.C D.D
2、填空题
15.化学是与大家的生产和生活紧密有关的学科,
(1)将以下物质的字母序号填在相应的空格内:
a.活性炭 b.小苏打 c.生石灰 d.尿素 e.烧碱 f.维生素A
①是化肥的是_____;
②缺少后会引起夜盲症的是_____;
③可用作食品干燥剂的是_____;
(2)有四种元素:A.铁元素 B.碘元素C.钙元素D.氧元素,请选择适合元素的字母序号填空:
①缺少后会引起贫血的元素是_____;
②地壳中含量最高的元素是_____;
③人体内含量最高的金属元素是_____.
16.请将下列物质的序号填在相应的空格内
①酚酞②过磷酸钙③钛合金④葡萄糖⑤橡胶⑥压缩天然气⑦石墨⑧二氧化碳
可用于制铅笔芯的是_____;
可以用作酸碱指示剂的是_____;
能作汽车燃料的是_____;
致使温室效应的主要气体是_____;
可制造车胎的是_____;
农业常见的磷肥是_____;
能为人体提供能量的物质是_____;
可制造“人造骨”的是_____。
17.化学与大家的生活息息有关。
(1)包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等。其中富含糖类的是_____,不含有有机物的是_____。
(2)老年人缺_____会发生骨质疏松,容易骨折。
(3)塑料盆、铁锅,陶瓷茶杯等是生活容易见到用品,其中是有机合成材料的是_____。
(4)活性炭能除去家装中产生的有害气体,这是借助了活性炭的_____性。
(5)加了洗涤剂的水能除去衣服上的油污,是借助了洗涤剂的_____用途。
(6)下列关于水的说法错误的是_____
A煮沸可以将硬水转化为软水
B工业废气直接排放会导致水污染
C探寻适合的催化剂,借助光照使水分解是理想的制氢办法
D很多用农药、化肥能提升农作物产量,不会导致水污染
(7)过氧化钙( CaO2) 可以用于鱼类运输时的制氧剂,与水反应生成碱和一种气体,写出反应的化学方程式_____。
(8)某注射用药液的配制办法如下:
①把 1.0g 药品溶于水配制成 4.0mL 溶液 a;
②取 0.1mL 溶液 a,加水稀释至 1.0mL,得溶液 b;
③取 0.1mL 溶液 b,加水稀释至 1.0mL,得溶液 c;
④取 0.4mL 溶液 c,加水稀释至 1.0mL,得溶液 d。
因为在整个配制过程中药液非常稀,其密度都可近似看做1g/cm3,1g 该药品可配制溶液d 的体积是_____mL。
18.用化学符号表示:
(1)两个氢原子
(2)三氧化硫中硫显+6价
(3)维持水的化学性质的最小粒子
(4)缺__________元素患侏儒症
(5)2个碳酸根离子
(6)3个亚铁离子
(7)含氧量最高的氧化物
(8)盐酸中的溶质__________.
3、判断题
19.A、B、C、D、E、X、Y、Z都是初中化学中的容易见到物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D、E是氧化物,常温下C是液体,Y是黑色固体,E是红色粉末。它们之间有如下反应关系:
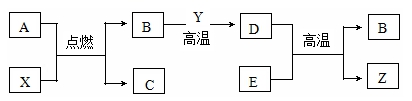
请依据以上信息回答下列问题:
(1)有关物质的化学式: X__________,C__________。
(2)B与Y反应的化学方程式为__________,
D与E反应的化学方程式为__________。
4、实验题
20.如图所示的是实验室制取蒸馏水的浅易装置,烧瓶和烧杯中都是自来水.
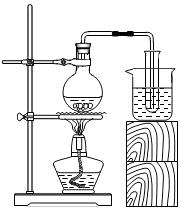
(1)酒精(C2H5OH)燃烧的化学方程式:____________.
(2)实验中消耗的40g酒精完全燃烧放出的热量为__________J.(酒精热值为3.0×107J/kg)
(3)实验结束后从试管和烧杯中各取10mL水,分别加入等量肥皂水,震动.察看到的现象是:_________
21.田老师为让学生更好理解蛋白质的“盐析”与“变性”,对教程实验进行改进并完成了如下实验.
序号 | 实验操作 | 实验现象 |
① | 在盛有鸡蛋清的试管中滴加饱和硫酸铵溶液 | 有白色絮状沉淀 |
② | 将①所得沉淀取出少许放入试管中,加入足量蒸馏水 | 沉淀完全溶解 |
③ | 在装有硫酸铵晶体的试管中加少量蒸馏水 | 沉淀完全溶解 |
④ | 在盛有鸡蛋清溶液的试管中滴加乙酸铅溶液 | 有沉淀 |
⑤ | 将④所得沉淀取出少许放入试管中,加入足量蒸馏水 | 沉淀未溶解 |
(1)实验①②③研究的蛋白质的特质是__________(填“盐析”或“变性”);
(2)补充实验②的目的是说明实验①中蛋白质发生的________(填“是”或“不是”)化学变化;
(3)设计对比实验①、③的目的是__________________________________;
(4)针对实验④,小黄同学提出了质疑:使蛋白质发生上述变化的是不是为重金属离子.请补充完成实验⑥,供选择的试剂有:鸡蛋清、蒸馏水、食盐水、硫酸铜溶液、浓硝酸.
序号 | 实验操作 | 实验现象 | 实验结论 |
⑥ |
|
| 重金属离子使蛋白质发生了变化 |
5、计算题
22.花青素(化学式![]() )具备缓解双眼疲劳,保护视力有哪些用途,该物质主要源自各种蔬菜和水果。
)具备缓解双眼疲劳,保护视力有哪些用途,该物质主要源自各种蔬菜和水果。
(1)花青素中碳、氢、氧元素的水平比为_____;
(2)花青素的相对分子水平为_____;
(3)花青素中氧元素的水平分数为_____(计算结果精准到0.1%)
23.现在市场上的补钙药剂不少,下图是某品牌补钙药品的部分说明书.

为测定其含量是不是达标,某兴趣小组的同学取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应):
加入稀盐酸的水平/g | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯中剩余物质水平/g | 10 | 29.12 | 48.24 | 67.36 | 86.48 | 106.48 |
请你依据题给信息和表中数据,回答下列问题:
(1)实验过程中将钙片研碎的目的是:__________.
(2)完全反应后,产生二氧化碳的水平为__________g.
(3)试通过计算说明,该品牌钙片含量是不是达标.(写出计算过程)
(4)假如按用量服用,服用者天天通过该补钙剂摄入钙元素的水平为__________g.
参考答案
1.C 2.D 3.B 4.C 5.A 6.B 7.B 8.B 9.D 10.A 11.D 12.A 13.A 14.D
15.d f c A D C
16.⑦ ① ⑥ ⑧ ⑤ ② ④ ③
17.面粉 食盐 钙/Ca 塑料盆 吸附 乳化 AD 2CaO2+2H2O=2Ca2+O2↑ 1000
18.2H;![]() ;H2O;Zn;2CO32﹣;3Fe2+;H2O2;HCl.
;H2O;Zn;2CO32﹣;3Fe2+;H2O2;HCl.
19.(1)O2H2O
(2)CO2+ C = 2CO 3CO + Fe2O3=2Fe + 3CO2
20.C2H5OH+3O2![]() 2CO2+3H2O 1.2×106J 试管中的水产生的泡沫较多,烧杯中的水产生的泡沫较少
2CO2+3H2O 1.2×106J 试管中的水产生的泡沫较多,烧杯中的水产生的泡沫较少
21.盐析 不是 证明实验①中析出的沉淀是蛋白质而不是硫酸铵 在盛有鸡蛋清溶液的试管中滴加硫酸铜溶液,取上述沉淀少许于试管中,加入足量的蒸馏水 有沉淀,沉淀未溶解
22.180:11:96 287 33.4%
23.(1)增大接触面积,使其充分反应;
(2)二氧化碳的水平=10g+100g﹣106.48g=3.52g;
(3)设碳酸钙的水平为x
![]()
100 44
x 3.52g
![]() x=8g
x=8g
所以药片中含碳酸钙的水平分数=![]() ,答:该品牌钙片含量达标.
,答:该品牌钙片含量达标.
(4)服用者天天通过该补钙剂摄入钙元素的水平=1g×2×80%×(![]() ×100%)=0.64g
×100%)=0.64g







